Cho 12,9 g hỗn hợp Fe, Mg, Zn phản ứng với 400 ml dung dịch X chứa HCl 1M và H2SO4 2M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch C và khí hydrogen
a) chứng tỏ rằng dung dịch C còn dư acid
b) Tính thành phần phần trăm khối lượng mỗi kim loại trong A. Biết số mol Mg trong A gấp 3 lần số mol Fe và tổng thể tích khi hydrogen sinh ra là 7,437 lít (đkc)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, Giả sử hỗn hợp chỉ gồm Zn.
Ta có: \(n_{Zn}=\dfrac{21}{65}\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Xét tỉ lệ: \(\dfrac{\dfrac{21}{65}}{1}>\dfrac{0,6}{2}\), ta được KL dư, mà nhh min → A không tan hết.
b, Sửa đề: Cu → CuO
\(n_{H_2}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\)
\(n_{CuO}=\dfrac{40}{80}=0,5\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,5}{1}>\dfrac{0,3}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{CuO\left(pư\right)}=n_{H_2}=0,3\left(mol\right)\Rightarrow n_{CuO\left(dư\right)}=0,2\left(mol\right)\)
⇒ m rắn = mCu + mCuO = 0,3.64 + 0,2.80 = 35,2 (g)

\(n_{H_2}=\dfrac{4,958}{24,79}=0,2\left(mol\right)\)
PTHH:
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
Do MgO, CuO, Fe2O3 có tỉ lệ mol = nhau, 1 mol Fe2O3 cần 3 mol H2 .
=> nMgO = nCuO= nFe2O3 = 0,05(mol)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
0,05 0,1
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
0,05 0,1
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
0,05 0,3
\(V_{HCl}=\dfrac{0,5}{1}=0,5\left(l\right)\)

\(n_{C_2H_2}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
\(C_2H_2+\dfrac{5}{2}O_2\rightarrow\left(t^o\right)2CO_2+H_2O\)
0,3 0,75 0,6 0,3
\(b,V_{O_2}=0,75.24,79=18,5925\left(l\right)\)
\(c,m_{CO_2}=0,6.44=26,4\left(g\right)\)
\(m_{H_2O}=0,3.18=5,4\left(g\right)\)

a:
\(n_{Al}=\dfrac{5.4}{27}=0,2\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,2 0,6 0,2 0,3
\(m_{AlCl_3}=0,2\left(27+35,5\cdot3\right)=26,7\left(g\right)\)
b: \(100ml=0,1\left(lít\right)\)
\(C_{M\left(HCl\right)}=\dfrac{0.6}{1}=0,6\left(\dfrac{mol}{lít}\right)\)
c: \(n_{H_2}=3\cdot\dfrac{0.2}{2}=0,3\left(mol\right)\)
=>\(V_{H_2}=0,3\cdot22,4=6,72\left(lít\right)\)

Chất X có 1 nguyên tử Cl nên X có công thức là \(Na_xCl\left(y=1\right)\)
Khối lượng phân tử chất X :
\(M=\dfrac{m}{n}=29,\dfrac{25}{0,5}=58,5\left(đvc\right)\)
mà \(M=23.x+35,5\)
\(\Rightarrow x=\dfrac{58,5-35,5}{23}=1\)
Vậy CTHH của X là NaCl

Ui hệ số trước \(H_2O\) là \(\dfrac{6-x}{2}H_2O\) mới đúng nha mik ghi nhầm í

\(m_{dd.muối.X}=3,2+196,8=200\left(g\right)\)
Có: \(C\%_X=\dfrac{m_X.100\%}{200}=4\%\Leftrightarrow m_X=8\left(g\right)\) \(M_2\left(SO_4\right)_n\)
\(3,2\left(g\right)M_2O_n\rightarrow8\left(g\right)M_2\left(SO_4\right)_n\)
=> \(n_{SO_4^{2-}}=\dfrac{8-3,2}{96-16}=0,06\left(mol\right)\)
\(C\%_{H_2SO_4}=\dfrac{0,06.98.100\%}{196,8}=2,99\%\)

a)
\(Na_2O+H_2O\rightarrow2NaOH\)
Nhúng giấy quý tím vào dung dịch thấy quỳ chuyển màu xanh.
b)
\(K_2O+H_2O\rightarrow2KOH\)
\(Al_2O_3+2KOH\rightarrow2KAlO_2+H_2O\)
Chất rắn tan dần tạo dung dịch trong suốt.
c)
\(SO_2+2H_2O+Br_2\rightarrow H_2SO_4+2HBr\)
Dung dịch brom bị mất màu.
d)
\(FeO+2HCl\rightarrow FeCl_2+H_2O\)
Chất rắn tan tạo dung dịch màu lục nhạt.

Gọi CTHH của acidic oxide đó là \(X_2O_n\)
\(\%m_X=100\%-56,34\%=43,66\%\)
Ta có : \(\dfrac{x}{2}=\dfrac{M_X}{\%m_X}:\dfrac{M_O}{\%m_O}\)
\(\Rightarrow\dfrac{x}{2}=\dfrac{M_X}{43,66\%}:\dfrac{16}{56,34\%}\)
\(\Rightarrow M_X=6,2n\)
Ta có bảng :
| n | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| \(M_X\) | 6,2 | 12,4 | 18,6 | 24,8 | 31 | 37,2 | 43,4 |
| Kết luận | Loại | Loại | Loại | Loại | P (thỏa mãn) | Loại | Loại |
Vậy \(X\) là \(P\) , A là \(P_2O_5\)
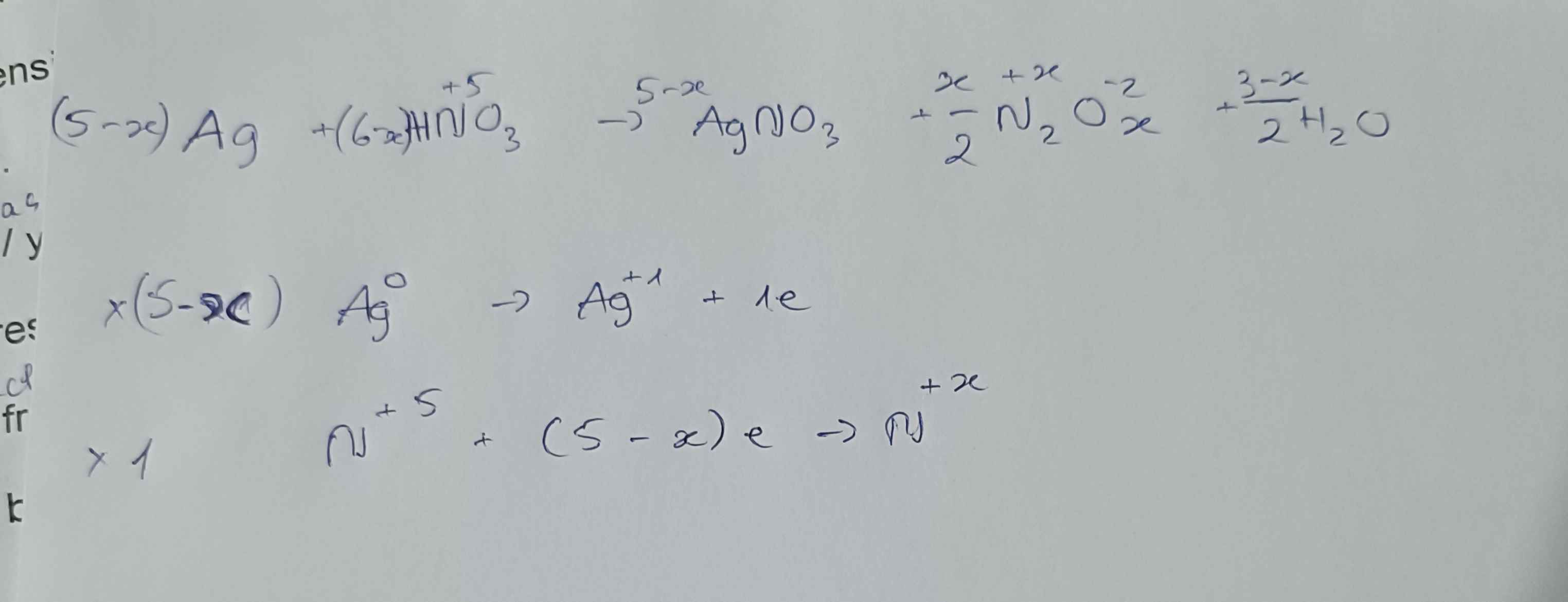
a, nH+ = nHCl + 2nH2SO4 = 0,4.1 + 2.0,4.2 = 2 (mol)
Giả sử hh chỉ gồm Mg.
\(\Rightarrow n_{Mg}=\dfrac{12,9}{24}=0,5375\left(mol\right)\)
Xét: \(Mg+2H^+\rightarrow Mg^{2+}+H_2\)
có \(\dfrac{0,5375}{1}< \dfrac{2}{2}\) ta được H+ dư, mà nhh max → dd C còn acid dư.
b, Gọi: \(\left\{{}\begin{matrix}n_{Mg}=3x\left(mol\right)\\n_{Fe}=x\left(mol\right)\\n_{Zn}=y\left(mol\right)\end{matrix}\right.\) ⇒ 3x.24 + 56x + 65y = 21,9 (1)
Có: \(n_{H_2}=n_{Mg}+n_{Fe}+n_{Zn}=3x+x+y=\dfrac{7,437}{24,79}=0,3\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,15\left(mol\right)\\n_{Fe}=0,05\left(mol\right)\\n_{Zn}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,15.24}{12,9}.100\%\approx27,9\%\\\%m_{Fe}=\dfrac{0,05.56}{12,9}.100\%\approx21,7\%\\\%m_{Zn}\approx50,4\%\end{matrix}\right.\)