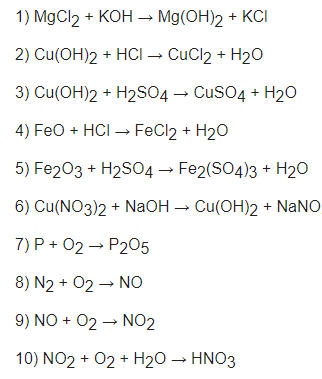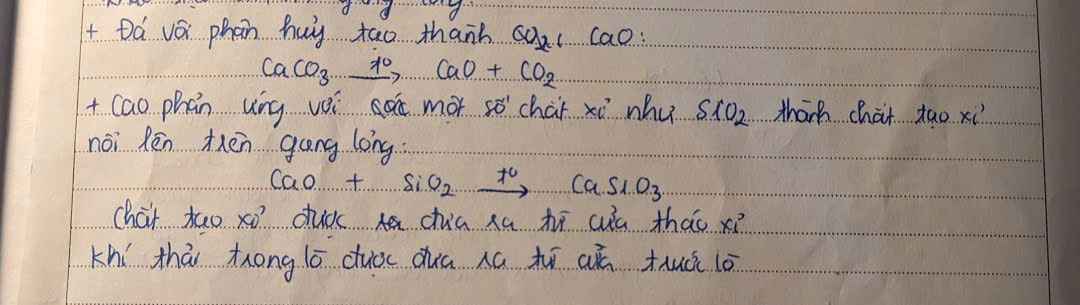Câu 5. Hòa tan hoàn toàn 10,4 gam hỗn hợp X gồm Zn và Fe trong dung dịch H2SO4 1M (được lấy dư), thu được 7,437 lít khí H2 (đkc). a. Tính số mol mỗi kim loại trong hỗn hợp X. b. Tính thể tích dung dịch H2SO4 đã tham gia phản ứng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(Mg+Cl_2\rightarrow MgCl_2\)
số mol của Mg là: \(n_{Mg}=\dfrac{m_{Mg}}{M_{Mg}}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
số mol của Cl2 là: \(n_{Cl_2}=\dfrac{V_{Cl_2}}{24,79}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
vì \(n_{Mg}=0,1=n_{Cl_2}\) nên sau phản ứng không có chất nào dư

Lượng nước cần cung cấp cho Hà Nội mỗi ngày là: V H 2 O = 8000000 . 200 = 1600000000 ( l ) = 1600000 ( m 3 ) Lượng clo cần xử lý là: m C l 2 ( C a n x u l y ) = 5 . 160000 = 8000000 ( g ) = 8000 k g

1) MgCL2 + 2KOH ==> Mg(OH)2 + 2KCl
2) Cu(OH)2 + 2HCl ==> CuCl2 + 2H2O
3) CuSO4 + H2SO4 ==> CuSO4 + 2H2O
4) FeO + 2HCl ==> FeCL2 + H2O
5) Fe2O3 + 3H2SO4 ==> Fe2(SO4)3 + 3H2O
6) Cu(NO3)2 + 2NaOH ==> Cu(OH)2 + 2NaNO3
7) 4P + 5O2 ==> 2P2O5
8) N2 + O2 ==> 2NO
9) 2NO + O2 ==> 2NO2
10) 4NO2 + 3O2 + 2H2O ==> 4HNO3

`#1194`
Qtr sx thép:
- Nguyên liệu: gang, sắt, thép phế liệu, khí oxygen
- Cách thực hiện:
+ Khí oxy được thổi từ dưới lò lên để đốt cháy tạp chất trong gang
+ Các oxide tạo thành ở dạng khí \(\left(\text{CO}_2;\text{ }\text{ SO}_2;...\right)\) sẽ thoát ra theo khí thải, các oxide dạng rắn \(\left(\text{SiO}_2;\text{ MnO}_2;...\right)\) sẽ tạo ra xỉ nhẹ, nổi lên trên thép nóng.
- Xỉ được tách ra để thu lấy thép.