Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Công thức về khối lượng phản ứng:
mCaCO3 = mCaO + mCO2
b) Áp dụng định luật bảo toàn khối lượng ta có :
mCaCO3 = 140 + 110 = 250 kg
Tỉ lệ phần trăm của Canxi cacbonat có trong đá vôi là :
%mCaCO3 = \(\frac{250.100\text{%}}{280}\) = 89,28%.

a) mCaCO3 = mCaO + mCO2
b) Khối lượng của CaCO3 đã phản ứng:
140 + 110 = 250 kg
Tỉ lệ phần trăm khối lượng CaCO3 chứa trong đá vôi:
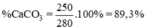

-
\(n_S:n_H:n_O:n_N=\dfrac{24,24\%}{32}:\dfrac{6,06\%}{1}:\dfrac{48,48\%}{16}:\dfrac{21,22\%}{14}=1:8:4:2\)
-
CTHH của X là (SH8O4N2)n
\(n_N=\dfrac{100}{14}=\dfrac{50}{7}\left(mol\right)\)
=> \(n_{\left(SH_8O_4N_2\right)_n}=\dfrac{\dfrac{50}{7}}{2n}=\dfrac{25}{7n}\left(mol\right)\)
=> \(m_{\left(SH_8O_4N_2\right)_n}=\dfrac{25}{7n}.132n=\dfrac{3300}{7}\left(g\right)\)
a, CTHH là SxHyOzNt
\(\rightarrow32x:y:16z:14t=24,24:6,06:48,48:21,22\)
\(\rightarrow x:y:z:t=\dfrac{24,24}{32}:\dfrac{6,06}{1}:\dfrac{48,48}{16}:\dfrac{21,22}{14}\)
\(\rightarrow x:y:z:t=1:8:4:2\)
=> CTHH: SH8O4N2
Hay (NH4)2SO4
b, \(n_N=\dfrac{100}{14}=\dfrac{50}{7}\left(g\right)\)
\(\rightarrow n_{\left(NH_4\right)_2SO_4}=\dfrac{50}{7.8}=\dfrac{25}{28}\left(g\right)\\ \rightarrow m_{\left(NH_4\right)_2SO_4}=\dfrac{25}{28}.132=\dfrac{825}{7}\left(g\right)\)

a) Công thức về khối lượng phản ứng:
mCaCO3 = mCaO + mCO2
b) mCaCO3 = 280 + 110 = 390 kg
=> %CaCO3
= \(\frac{390}{560}\) = 69,7%

$\%m_{O_2(X)}=\dfrac{1,6}{1,6+4,4}.100\%=26,67\%$
$n_{CO_2}=\dfrac{4,4}{44}=0,1(mol);n_{O_2}=\dfrac{1,6}{16}=0,05(mol)$
$\Rightarrow \%V_{O_2(X)}=\dfrac{0,05}{0,05+0,1}.100\%=33,33\%$
$C+O_2\xrightarrow{t^o}CO_2$
Theo PT: $n_C=n_{O_2(p/ứ)}=n_{CO_2}=0,1(mol)$
$\Rightarrow n_{O_2(dùng)}=0,1+0,05=0,15(mol)$
$m_C=0,1.12=1,2(g);V_{O_2(dùng)}=0,15.22,4=3,36(lít)$
$\to m=1,2;V=3,36$

Công thức :
\(M_2O_n\)(với n là hóa trị của nguyên tố M)
ta có:
\(\%m_M=\frac{2\cdot M_M}{2\cdot M_M+n\cdot16}\cdot100=60\)
ta thấy \(n\in\left\{1;7\right\}\)
| n | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| MM | 12 | 24 | 36 | 48 | 60 | 72 | 84 |
| Thử | loại | Mg (thỏa mãn) | loại | Ti | loại | loại | loại |
Có sai mong bạn thông cảm ah

CHÚC BẠN HỌC TỐT!![]()
![]()
![]()
Câu 1+3: Mình không hiểu đề cho lắm!!?
Câu 2: Gọi CTHH của X là CxHy
Theo đề bài, ta có:
+) \(PTK_X=\dfrac{7}{8}PTK_{O2}\) \(\Rightarrow PTK_X=32.\dfrac{7}{8}=28\)
+) \(\%C=85,71\%\Rightarrow\%H=14,29\%\)
\(\Rightarrow\left\{{}\begin{matrix}\%C=\dfrac{12x}{28}.100\%=85,71\%\\\%H=\dfrac{y.1}{28}.100\%=14,29\%\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=4\end{matrix}\right.\)
Vậy CTHH của X là C2H4
Bài 1 :
Ta có :
PTKH2S = PTKH2 + PTKS
=> PTKH2S = 2 đvC + 32 đvC
=> PTKH2S = 34 đvC
=> Tỉ số phần trăm của H trong H2S là :
2 : 34 * 100% = 5,88%
=> Tỉ số phần trăm của S trong H2S là :
32 : 34 * 100% = 94,12%
Bài 2 :
Ta có : PTKH2SO4 = PTKH2 + PTKS + PTKO4
=> PTKH2SO4 = 2 đvC + 32 đvC + 64 đvC
=> PTKH2SO4 = 98 đvC
=> Tỉ số phần trăm của H trong H2SO4 là :
2 : 98 * 100% = 2,04%
=> Tỉ số phần trăm của S trong H2SO4 là :
32 : 98 * 100% = 32,65%
=> Tỉ số phần trăm của O trong H2SO4 là :
64 : 98 *100% = 65,31%
Bài 1 :
Ta có :
PTKH2S = PTKH2 + PTKS
=> PTKH2S = 2 đvC + 32 đvC
=> PTKH2S = 34 đvC
=> Tỉ số phần trăm của H trong H2S là :
2 : 34 * 100% = 5,88%
=> Tỉ số phần trăm của S trong H2S là :
32 : 34 * 100% = 94,12%
Bài 2 : PTKH2SO4 = PTKH2 + PTKS + PTKO4
=> PTKH2SO4 = 2 đvC + 32 đvC + 64 đvC
=> PTKH2SO4 = 98 đvC
=> Tỉ số phần trăm của H trong H2SO4 là :
2 : 98 * 100% = 2,04%
=> Tỉ số phần trăm của S trong H2SO4 là :
32 : 98 * 100% = 32,65%
=> Tỉ số phần trăm của O trong H2SO4 là :
64 : 98 *100% = 65,31%